معالجة المياه مهمة وهي المعالجة المسبقة للغلاية. يمكنه إزالة قلوية الكربونات في مياه التغذية قبل أن تصل إلى المرجل. في الماء المغلي ، الحد الأول للمعلمة الكيميائية هو القلوية. من خلال تقليل القلوية ، يمكن أن يساعد على تقليل أحجام التفوت ، وزيادة دورات التركيز وتقليل استهلاك الطاقة. هنا سوف نقدم القلوية ولماذا نحتاج إلى تقليل القلوية و كيفية إنتاج مياه التبيلات.
تشير القلوية إلى قدرة الماء على تحييد الأحماض ، يتحدد أساسًا بتركيز الكربونات (CO32-) ، بيكربونات (HCO)3-هيدروكسيد (أوه)-أيونات موجودة في الماء. يعكس إجمالي كمية المواد في الماء التي يمكن أن تعمل كمخازن قاعدة حمضية وتقاس عادة بجزء في المليون (أجزاء في المليون) أو ملغم/لتر.
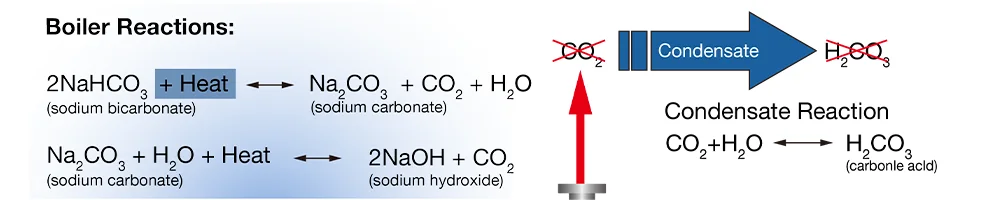
القلوية التي تحدث بشكل طبيعي في الماء الخام تأتي في شكل كربونات وبيكربونات. عندما تدخل القلوية الغلاية ، فإنها تنهار إلى أوه- و CO2. CO2 يتم تفريغ (الغاز) مع البخار ويشكل حمض الكربونيك كما يتكثف البخار (pH<6.0). إن الماء ذو القلوية غير معالج ، الماء المنخفض pH يمكن أن يتآكل شبكة المكثفات وخطوط الأنابيب.

يمكن أن يكون للمياه القلوية آثار سلبية مختلفة على الإنتاج الصناعي:
تعتمد عملية إزالة المياه الرئيسية مبادئ التبادل الأيوني ، أي إزالة أيونات الكربونات والبيكربونات مع راتنجات التبادل الأيوني للكيس أو الوبر أو السبا لتحقيق معالجة المياه. هناك ثلاث طرق رئيسية لإكمال عملية تحويل المياه ، هنا سنقدمها لك واحدًا تلو الآخر ونمنحك مقارنة لمساعدتك في العثور على نظامك المناسب واختيار راتنجات التبادل الأيوني الصحيح.
Dealization أنيون كلوريد. طريقة دورة Choride تشبه تمامًا عملية تليين المياه ، التي تتبادل أيونات تسخير (Ca+، ملغ+، وما إلى ذلك) مع الأيونات + نا في التبادل الأيوني. يعتمد نظام دورة Choride على راتنجات قاعدة أنيون قوية (SBA) لإكمال التبادل الأيوني. يدخل الماء القلوي مع الكربونات والبيكربونات إلى الخزان ويمر عبر راتنجات التبادل الأيوني ، ويتم تبادل الكربونات والبيكربونات مع أيونات الكوريدي على الراتنجات. ثم تتم إزالة القلوية وتبقى فقط أيونات Choride في الماء. بمجرد أن تكون الراتنجات معكوسة ، فإنها تحتاج إلى إعادة توليدها باستخدام كلوريد الصوديوم (NaCl) أو محلول مركب ملح كاوي (NaOH). في هذا النظام ، يتم استخدامه بشكل شائع مع راتنجات كيس (كاتيون حمض قوي) للتليين.


انقسام تيار dealization. تستخدم هذه الطريقة مفاعلين كاتيونتين حامضية قوية متوازية (كيس). مفاعل واحد يعمل بالصوديوم (غ+شكل ، إزالة الصلابة مع الحفاظ على 100% من القلوية ، بينما يعمل الآخر في الهيدروجين (H+) شكل ، إزالة كل القلوية ولكن تبقى حموضة المعادن الحرة (FMA). في الخطوة nex ، مزيج هذين التيارين ، FMA في راتنجات الهيدروجين الكاتيلة أغطية النفايات السائلة كربونات الصوديوم وقلوية البيكربونات في راتنجات الصوديوم الكاتيونية النفايات السائلة إلى حمض الكربونيك. الرجوع إلى رد الفعل التالي:

ثم ، يتفكك حمض الكربونيك المتولد في الماء (H2س) وثاني أكسيد الكربون (CO2) ، وسيتم تسليمها إلى ديغاسيفير لإزالة ثاني أكسيد الكربون من خلال تيار الهواء المعاكس. يمكن التحكم في قلوية الماء النهائية عن طريق إدارة النسبة المئوية لكل تدفق مياه مختلط.

ملخص مقارن
| الطريقة | المزايا | عيوب | سيناريوهات التطبيق |
|---|---|---|---|
| كلوريد دورة dealization | يزيل القلوية بفعالية ؛ مناسبة للتطبيقات الصناعية | التجديد قد يدخل أيونات الكلوريد ؛ الإدارة المطلوبة | معالجة المياه الصناعية. يمنع تحجيم المرجل |
| Dealization حمض ضعيف | مزايا تكلفة كبيرة ؛ نفايات سائلة عالية الجودة ؛ لم يتم إدخال أيونات إضافية | معالجة بطيئة نسبيًا ؛ تطبيق محدود | حالات ذات نسب عالية من الصلابة إلى القلوية |
| انقسام تيار dealization | تعديلات مرنة للقلوية المتدفقة ؛ ارتفاع الاستقرار والقابلية للتكيف | تصميم نظام معقد ؛ يتطلب مراقبة ومراقبة عالية | التعامل مع نوعية مياه متباينة ؛ معالجات قابلة للتكيف |
يعد اختيار طريقة المناسبة أمرًا مهمًا لتحسين فعالية معالجة المياه وتقليل تكاليف الإنتاج وضمان جودة المنتج. من خلال فهم مزايا وعيوب العمليات المختلفة ، يمكن للمؤسسات الصناعية اتخاذ قرارات مستنيرة بناءً على احتياجاتها الخاصة.